类风湿关节炎(专业版)
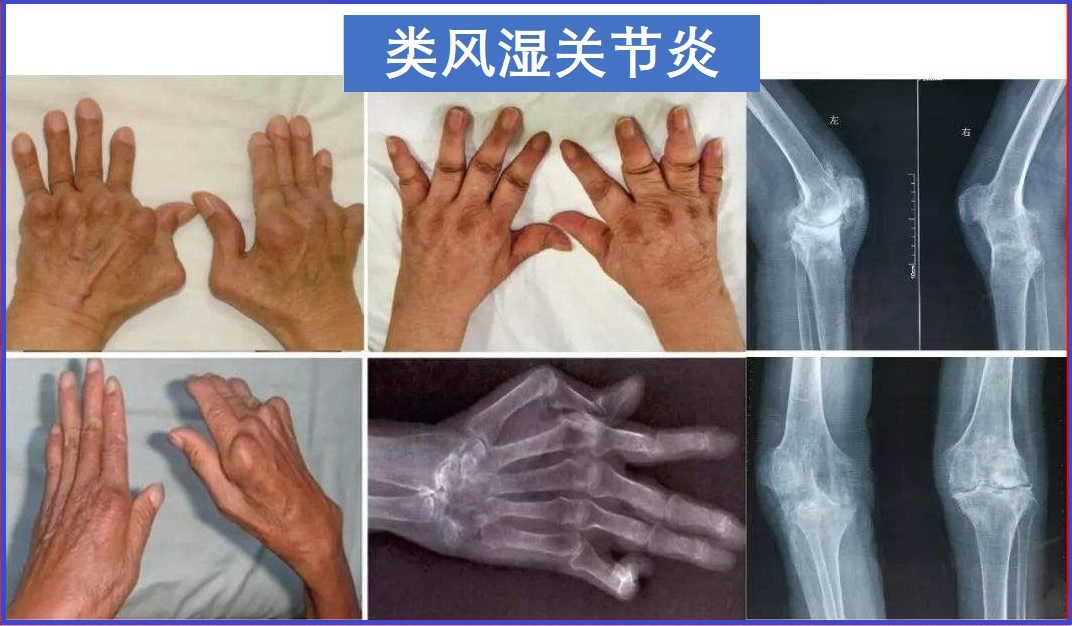
类风湿关节炎(RA)是一种原因未明的慢性、以炎性滑膜炎为主的系统性疾病。主要表现为手、足小关节的多关节、对称性、侵袭性炎症,引起周围关节疼痛、肿胀、僵硬和功能丧失。
定义
类风湿关节炎(RA)是一种原因未明的慢性、以炎性滑膜炎为主的系统性疾病。主要表现为手、足小关节的多关节、对称性、侵袭性炎症,引起周围关节疼痛、肿胀、僵硬和功能丧失。作为全身性、炎症性疾病,它尤其显著增加了心血管疾病的风险。常规治疗多集中在症状方面,而忽视了系统性炎症对健康造成的更大损害。有研究表明,与健康人相比,患有RA的个体死亡风险增加了近40%。类风湿关节炎症状和严重程度一般有3种模式:
- 自发性缓解:症状最终消失,发生在不到10%的RA患者中。
- 复发或缓解型:患者经历了称为“耀斑”的非常严重症状的时期,与轻度或无症状发作形成对比。这种模式通常在RA早期发生。
- 持续和进展性型:疾病逐渐恶化,但是,耀斑和缓解期并不像复发型那样剧烈。这是最常见的RA疾病过程。
病因
RA是由基因因素和环境因素共同作用引起的。可能的原因包括如下:- 基因因素,患者可能会有一个特定的基因缺陷,增加患该疾病的风险。
- 免疫系统的缺陷,导致免疫细胞不能识别自身组织。
- 感染特定病毒或细菌,引起异常的免疫应答。
- 激素或生化失衡。
风险因素
RA在女性以及30-60岁的人群中较易发生。其他可能增加RA发生几率的因素包括:
- 家庭成员患有RA。
- 超重或肥胖 。
- 重度或长期吸烟。
症状
RA症状通常表现在关节,包括如下:- 症状通常涉及2个或更多的关节:
- 身体较小的关节
- 在身体两侧同样的关节
- 症状包括:
- 在早晨疼痛和僵硬增加
- 关节肿胀,发红、发热
- 关节变形或畸形
- RA还可能导致如下症状:
- 连续性疲劳,缺乏活力
- 肌肉酸痛
- 食欲下降
- 体重下降
- 发烧和盗汗
- 失眠
- 皮肤下小肿块或结节
- 炎症也可能出现在:
- 眼睛
- 口腔
- 皮肤
- 肺部
- 血液和血管
并发症
类风湿性关节炎可能产生以下并发症:- 骨质疏松症:RA本身以及用于治疗类风湿性关节炎的一些药物可增加患骨质疏松症的风险。
- 类风湿结节:这些硬块通常形成在压力点附近,如肘部。但是,也可在身体的任何部位形成,包括肺部。
- 眼睛和嘴巴干燥:RA患者更容易患上干燥综合征,这种疾病会降低眼睛和口腔中的水分含量。
- 感染:RA及其治疗药物可损害免疫系统,导致感染风险增加。
- 身体组成异常:即使在体重指数正常的人群中,RA患者的脂肪与瘦体重的比例也较高。
- 心脏问题:RA可引起动脉硬化和阻塞,以及心包炎。
- 肺部疾病:RA可增加肺炎和瘢痕形成,导致呼吸困难。
- 淋巴瘤:RA可增加淋巴瘤(血癌)风险。
疗法
类风湿关节炎没有治愈的方法。治疗的目标是缓解疼痛、抑制炎症,降低关节损害,以及改善功能性能力。
综合选项可包括如下:
调整饮食和生活方式
- 健康饮食,如地中海饮食法。
- 不吸烟,或戒烟。
- 限制饮酒,或不饮酒。
- 经常做有氧运动,如游泳、步行等,可降低炎症、缓解疼痛。
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控类风湿关节炎(RA)的营养和草本补充剂,主要包括如下:
1.多不饱和脂肪酸:
多年来,主要来源于海洋的多不饱和脂肪酸(PUFA)一直被推荐用于RA患者,因为它们能够减少炎症,增强心血管健康,同时有助于舒缓过度活跃的免疫系统1。
膳食PUFA主要有两种类型:ω-6和ω-3,两者对健康都很重要。然而,在饮食中保持ω-6和ω-3的正确比例尤为重要。研究表明,现代人一般饮食中ω-6与ω-3的比例高达25:12。然而,理想的比例约为4:1,这意味着很少有人能获得足够的ω-3脂肪酸(相对于ω-6含量)3。如此偏向ω-6的比例有可能高度促炎。因此,关节炎患者必须获得足够的ω-3脂肪酸。
1.1.鱼油:
许多试验支持RA患者食用鱼油形式的ω-3脂肪酸益处。这些研究表明,鱼油有助于减轻炎症4、疼痛和RA相关症状。EPA和DHA来源于鱼油,已被证明具有抗炎特性。一项研究的结果表明,RA患者在三个月内每天摄入1800mg EPA和900mg DHA,这些脂肪酸可以有效控制晨僵,而服用安慰剂的患者症状恶化5。
许多临床研究支持RA患者食用鱼油的益处6。在一项评估关节压痛和控制严重RA患者症状所需非甾体抗炎药(NSAIDs)剂量的研究中,食用鱼油的患者关节疼痛较少,服用的非甾体类抗炎药剂量较低7。另一项研究的数据表明,食用鱼油可以增强对乙酰氨基酚的抗炎特性8。食用鱼油还能显著降低TNF-α和其他促炎细胞因子9。鱼油还显著改善了RA患者的胆固醇和甘油三酯水平,降低了心血管风险10。
1.2.磷虾油:
其性质与鱼油略有不同。在动物模型中,磷虾油“显著降低了关节炎评分和肿胀”11。在另一项关于磷虾油、透明质酸和虾青素结合的临床研究中,关节炎患者报告称,在不到三个月的时间里,疼痛减轻了55%。63%的参与者在治疗后完全没有疼痛12,13。
1.3.γ-亚麻酸(GLA):
GLA是一种有益的ω-6脂肪酸,存在于几种不同植物的油中。它对心脏健康的影响是有据可查的。在一项研究中,RA患者每天摄入1400mg GLA,他们的RA症状显著减轻,包括关节疼痛的数量和严重程度以及肿胀程度14。对临床试验的彻底审查发现,尽管每天摄入1400mg或更多的GLA可显著改善RA相关症状,但较低剂量(即每天500mg)似乎没有效果15。其他研究表明,以下富含GLA的油可能对RA患者有益:
- 黑加仑籽油:一项涉及RA患者的24周临床试验将黑加仑油与安慰剂的效果进行了比较,发现黑加仑籽油显著改善了RA相关症状16。
- 琉璃苣油:从琉璃苣植物种子中提取的油富含GLA。在测试GLA在减少RA症状方面的益处的研究中,硼砂籽油被用作GLA的来源14。一项综合综述的结果表明,琉璃苣籽油与RA患者的临床结果改善有关17。
- 月见草油:一项综述表明,月见草有效地减轻了RA症状20。在一项研究中,RA患者每天服用NSAIDs治疗,每天服用6g月见草油或安慰剂。接受每日剂量月见草油的患者在3个月后晨僵减轻,6个月后疼痛减少21。
2.内源性化合物
2.1.S腺苷蛋氨酸(SAMe):
SAMe是体内的一种天然化合物,对许多不同的生理过程都是必需的。SAMe已被证明可以改善骨关节炎、肝病甚至抑郁症的症状。尽管大多数科学研究都集中在骨关节炎上,但SAMe的机制表明其在RA中发挥作用。SAMe支持软骨结构成分的产生,软骨结构成分可被RA的慢性炎症破坏。SAMe的抗炎特性表明该化合物在RA患者中具有支持作用22。
对几项个体临床研究的全面综述发现,SAMe减轻了骨关节炎患者的疼痛,改善了关节功能23。事实上,SAMe与NSAIDs治疗具有相似的镇痛和功能改善作用,但没有不良反应24。
此外,常见的RA药物甲氨蝶呤已被证明通过SAMe途径抑制细胞信号传导25。因此,关节组织中的细胞可能无法正常处理SAMe。这项实验室研究表明,接受甲氨蝶呤治疗的人可能会从补充SAMe中受益。
2.2.氨基葡萄糖(氨糖):
氨糖(如硫酸氨糖或盐酸氨糖)是糖胺聚糖的前体,糖胺聚糖是整合到软骨中的大分子蛋白聚糖的组成部分。蛋白聚糖对健康的软骨和关节的适当缓冲至关重要,因为它们能将水吸入关节,起到润滑剂的作用。此外,氨糖似乎具有一些抗炎特性22。
氨糖已被证明可抑制滑膜细胞中促炎细胞因子IL-8的产生26。另一项研究发现,尽管CRP等传统炎症标志物没有可检测的差异,但氨糖在显著减轻RA症状方面是有效的27。
2.3.硫酸软骨素:
软骨素是软骨的一种结构成分。当作为补充剂服用时,它有助于对抗炎症并支持软骨重建22。软骨素可能对心脏也有益。动脉粥样硬化和慢性关节炎的动物模型发现硫酸软骨素可以阻止动脉粥样硬化病变的发展28。这些数据虽然非常初步,但提出了硫酸软骨素可能有助于对抗RA中导致关节和心脏病的全身炎症的可能性。
3.维生素类:
3.1.维生素K:
维生素K是一种抗氧化剂和抗炎剂,在骨代谢和凝血中发挥作用,实际上是一组密切相关的化合物,包括维生素K1(叶绿醌)和维生素K2(甲萘醌)。维生素K1在食物中含量更高,但其生物活性不如维生素K2,后者还有许多不同的亚型。甲萘醌-4(MK-4)和甲萘醌-7(MK-7)是维生素K2最重要的形式。甲萘醌类主要存在于动物器官中,如肝脏,或细菌发酵食品中,如大豆、酸奶和奶酪29。
动物研究表明,口服维生素K在参与炎症途径的基因表达中发挥作用30。一项针对500多名老年人的为期一年的研究发现,饮食中摄入叶绿醌与胰岛素抵抗和慢性炎症性疾病相关标志物的改善有关31。细胞和动物研究表明,MK-4抑制大鼠类风湿性滑膜细胞的增殖,并抑制胶原诱导的关节炎32。
在一项针对158名未服用华法林或特立帕肽的女性RA患者的横断面研究中,70名患者接受了45mg/天的维生素K2治疗。与未接受治疗的组相比,治疗组的炎症标志物水平较低,包括CRP。此外,这项研究的一个纵向组成部分检查了52名服用维生素K和药物三个月的患者。这些患者的血清CRP在统计学上显著下降33。
在一项针对84名接受RA治疗的受试者的随机对照试验中,与对照组相比,每天服用100µg MK-7的组炎症标志物减少。MK-7的半衰期比MK-4更长,生物利用率更高34。维生素K具有对抗炎症和改善关节健康的潜力,尽管需要进一步的研究。
3.2.维生素D:
当皮肤接触紫外线时合成的维生素D发挥着重要的免疫调节作用,似乎可以明显缓解RA症状。一项随机临床试验的结果显示,与仅接受抗风湿药(DMARD)治疗的组相比,服用低剂量1-25二羟基维生素D及其疾病改良性DMARD药治疗的RA患者在3个月时的疼痛缓解明显更大35。令人担忧的是,瑞士最近的一项试验发现,272名RA患者中有86%的人维生素D缺乏或不足36。
维生素D受体(VDR)位于免疫细胞表面。由于免疫细胞在促进RA炎症中发挥着重要作用,维生素D在RA介导的炎症中也发挥作用似乎是合乎逻辑的。事实上,最近的一项研究发现,VDR在限制RA小鼠模型中免疫细胞的炎症倾向方面很重要37。
然而,维生素D的作用不仅仅是阻止破坏性免疫细胞,它还能增强保护性免疫细胞。T-reg细胞是免疫系统的特殊组成部分,有助于保持免疫平衡。如果T-reg细胞过少,免疫系统就会变得过度活跃,就像RA等自身免疫性疾病一样。维生素D增加了保护性T-reg细胞的数量,恢复了过度活跃的免疫系统的平衡38。
3.3.维生素B6:
RA患者维生素B6缺乏的患病率升高。这种缺乏与更严重的症状有关39。一项研究发现,每天服用100mg维生素B6可以降低RA患者血液中TNF-α和其他促炎细胞因子的水平40。
3.4.叶酸:
叶酸缺乏症在接受甲氨蝶呤治疗的RA患者中尤其常见,因为这种药物会消耗叶酸41。因此,补充叶酸可能对RA患者有益。
4.植物和植物衍生化合物:
4.1.穿心莲:
从穿心莲中提取的成分穿心莲内酯可抑制诱导型一氧化氮合酶(iNOS)的促炎活性。这有助于发挥强大的抗炎作用42。与对血管有益的eNOS(内皮NOS)不同,iNOS是促炎性的,并且经常涉及需要抑制其作用的疾病状态。
穿心莲内酯也抑制促炎细胞因子TNF-α和前列腺素E2(PGE-2)的产生,在多个水平上阻止其基因表达43,44。因此。它们下调了细胞用来相互“告知(To tell)”启动炎症反应的化学信号通路,而炎症反应在RA中起着关键作用45。
科学分析进一步表明,穿心莲内酯通过阻断促炎转录因子核因子κB(NF-kB)的作用,在炎症级联过程中“上游(Upstream)”发挥作用46。
NF-kB几乎存在于所有的人类细胞中。它在细胞对压力、细胞因子、自由基、氧化低密度脂蛋白(LDL)以及细菌或病毒病原体的反应中发挥着关键作用。因此,它作为氧化损伤、感染和毒素诱导的压力的第一反应者的核心作用将其与炎症、癌症和慢性病联系起来47。NF-kB几乎严格调节炎症级联反应下游的所有因子,包括白介素类细胞因子、前列腺素类激素和TNF-α。
通过阻断NF-kB,穿心莲内酯在一个简单的步骤中抑制了大量炎症介质的产生48。正如动物研究所证明的那样,它们还允许重要免疫监测细胞的正常活动,同时抑制过度活跃的炎症细胞49。
这是穿心莲内酯区别于大多数抗风湿药物(DMARDS)的关键特征。穿心莲内酯抑制炎症免疫因子,而DMARD通常会抑制免疫功能,导致感染风险增加50。
4.2.姜黄素:
姜黄素具有强大的抗氧化、抗炎和免疫调节特性。一项基于实验室的研究表明,姜黄素可以减少滑膜炎症51。具体而言,这项研究发现,将发炎的滑膜细胞暴露于姜黄素不仅降低了这些细胞的炎症状态,而且抑制了促炎蛋白的产生和具有炎症特性的细胞的激活。
姜黄素还有助于保护软骨免受炎症介导的破坏。一项荟萃分析试图检验姜黄素对软骨细胞(构成软骨的细胞)影响的大量证据。研究人员得出结论,姜黄素不仅有助于防止关节中某些炎症蛋白诱导的软骨降解52,而且有助于促进软骨再生53。
姜黄素也可能有助于降低治疗效果和药物相关肝毒性所需的甲氨蝶呤剂量。一项研究发现,在关节炎小鼠模型中,使用姜黄素和非常低的亚治疗剂量的甲氨蝶呤可以有效地治疗炎症,同时降低药物诱导的肝损伤水平54。如果姜黄素和甲氨蝶呤对人类同样有效,那么RA患者可以服用较低剂量的甲氨蝶啶,从而降低肝毒性的风险。
一项规模较小(18人)但设计良好的研究发现,食用姜黄素可以改善行走(增加时间),并显著减少关节肿胀和晨僵55。这些结果得到了一项更大规模的临床试验的证实,在该试验中,45名RA患者被随机分配接受50mg双氯芬酸和500mg高吸收形式的姜黄素,或同时接受这两种药物,为期8周。在这项试验中,通过多项标准化评估,姜黄素单独使用和与双氯芬酸联合使用在缓解RA疾病活性方面至少与双氯芬酸单独使用一样有效。此外,姜黄素单独对CRP(血液中炎症的标志物)的抑制作用比基线高52%,而单独使用双氯芬酸只降低了1.5%的CRP:“综合来看,我们目前的研究结果为姜黄素的优越性提供了一个明确的原理证明,并且当与双氯芬酸联合使用时,缺乏任何协同或相加功效,这强烈支持单独使用姜黄素在临床环境中安全有效地用于治疗RA,以及未来包括癌症在内的其他促炎疾病。”56。
4.3.槲皮素:
槲皮素可强烈抑制炎症过程的多种成分,包括NSAIDs药靶向的环氧合酶(COX)57。滑膜细胞的实验室实验表明,尽管槲皮素对促炎蛋白的产生没有影响,但它直接减少滑膜中的炎症以及促炎细胞的激活51。
最近的一项概念验证研究表明,在RA大鼠模型中,利用生物工程技术提高槲皮素的生物利用度,可以减少炎症。研究人员将槲皮素装载到微球中,并将微球-槲皮素组合直接输送到关节中58。微球使槲皮素能够在30天内持续释放。尽管还需要更多的人体试验,但迄今为止的数据支持槲皮素在RA中的抗炎作用。
4.4.乳香:
乳香含有活性的3-乙酰基-11-酮-β-乳香酸(AKBA),以及高水平的乳香酸,这些是5-脂氧合酶(5-LOX)的有效抑制剂,5-LOX是一种产生炎性白三烯的酶。乳香提取物也可能对促炎蛋白如TNF-α具有抑制作用59。在RA动物模型中,乳香提取物已被证明可以改善关节炎症状,降低炎症活性和标志物60,61。乳香在阿育吠陀医学中历来被用于治疗RA等炎症性疼痛疾病62。
一项针对260名RA参与者的安慰剂对照临床研究发现,乳香提取物有效改善了关节肿胀、疼痛和僵硬等症状;它还改善了红细胞沉降率,表明炎症有所改善63。另一项针对182名RA患者的安慰剂对照研究发现,与安慰剂相比,阿育吠陀植物提取物(包括乳香)联合治疗16周可改善关节肿胀64。
4.5.石榴:
石榴多酚是具有强大抗氧化性能的化合物。一项研究测试了在食物中添加石榴提取物的小鼠的炎症严重程度和关节炎发病率。石榴喂养组的小鼠关节炎的发病率较低,那些患关节炎的小鼠比正常情况下发病较晚(即延迟性疾病),关节炎症和损伤也有所减轻65。
在最近的一项试验研究中,石榴提取物对6名RA患者的疗效进行了测试,据报道,服用石榴提取物的人关节疼痛明显减少66。扩大所研究患者的样本量将决定这些影响是否广泛适用。
4.6.生姜:
生姜具有强大的抗炎和抗氧化特性67。生姜通过抑制促炎酶和阻断促炎蛋白的产生直接抑制炎症68。此外,几位研究人员报告称,食用生姜可以显著预防RA啮齿动物模型中关节炎的发作69-71。
4.7.黑籽油:
黑籽油来源于 “黑孜然(Nigella sativa)”或“黑香菜”籽。研究表明,在RA大鼠模型中,喂食黑籽油的活性化合物胸腺醌可以抑制炎症并预防关节炎72。
最近的一项研究比较了RA患者在一个月内每天两次服用500mg黑籽油与安慰剂的症状。值得注意的是,高达40%(根据用于评估症状的疾病活动量表,差异约为10%)的服用黑籽油的患者RA症状有所改善73。
4.8.β-谷甾醇和β-谷甾醇糖苷:正如一些初步研究所表明的,一种名为Moducare®的β-谷甾醇(BSS)和β-谷甾醇糖苷(BSSG)的99:1专有混合物可能调节RA的免疫力。在实验室研究中,BSS/BSG混合物已经证明了在不同条件下平衡免疫细胞功能的能力74,75。
两项针对人类受试者的小型试点研究证实了体外数据。在第一项研究中,17名超级马拉松运动员接受了BSS/BSG混合物或安慰剂治疗。比赛结束后,当免疫功能通常发生剧烈变化时,研究人员评估了两组的炎症参数。在服用BSS/BSG混合物的组中,注意到免疫细胞水平升高,而血液中的炎症介质下降,这表明混合物在抑制过度炎症的同时为免疫系统防御做好了准备76。在第二项试验中,18名活动性RA患者服用BSS/BSG混合物或安慰剂24周。与安慰剂相比,该混合物在以下所有方面都有显著改善:可测量的软关节计数、患者对疼痛的评估、患者对疾病活动的总体评估,以及医生对疼痛的总体评估。此外,评估血液炎症倾向的红细胞沉降率(ESR)下降了56%77。
更多内容可点击其个性化的综合干预方案如下:
- 类风湿防控要略(抑制自体免疫)
- 类风湿防控要略(保护关节)
- 类风湿防控要略(抗肿止痛)
- 类风湿防控要略(局部抗肿)
- 类风湿防控要略(减少过敏原)
- 类风湿关节炎防控(25-35岁)
- 类风湿关节炎防控(36-45岁)
- 类风湿关节炎防控(46-55岁)
- 类风湿关节炎防控(56-65岁)
- 类风湿关节炎防控(66岁以上)
以及参阅本网如下专文的有关内容:
医疗干预
常规治疗包括如下:
- 非处方或处方非甾体类抗炎药(NSAIDs),如布洛芬、环氧合酶-2、COX-2抑制剂。它们可应用于皮肤或由口腔服用。
- 抗类风湿药(DMARDs),减缓病情,口服或皮下注射:
- 非生物免疫抑制剂,最常见的是甲氨喋呤。
- 生物制剂,旨在修复、刺激或增强免疫系统。常见的生物DMARDs包括阿达木单抗,依那西普和阿贝西普。
- 糖皮质激素,注入关节中(较少用)。
自我护理
- 休息和合适的运动:休息可以减少关节炎症、僵硬、疼痛和抗疲劳。运动对于保持肌肉力量和柔韧性很重要,并可维持关节的灵活性。
- 注意休息和锻炼之间的平衡
- 尝试温和的力量训练
- 参加有氧运动,如步行、游泳、跳舞
- 避免重冲击运动
- 控制体重
- 参与物理治疗计划
- 关节护理:使用夹板可以减轻关节疼痛。帮助日常活动的设备能减少对关节的压力,包括:
- 拉链延长器
- 长柄鞋拔
- 专门设计的厨房工具
- 降低压力:压力降低可以缓解与慢性病和疼痛相关的生活困难,可以咨询专业人士具体方法。
预防
还没有预防类风湿关节炎的指南。
参考文献:
1. Goldberg RJ et al. A meta-analysis of the analgesic effects of omega-3 polyunsaturated fatty acid supplementation for inflammatory joint pain. Pain, 2007. 129(1-2):210-23.
2. Simopoulos AP. Evolutionary aspects of diet: the omega-6/omega-3 ratio and the brain. Mol Neurobiol. 2011 Oct;44(2):203-15. Epub 2011 Jan 29.
3. Holub BJ. Clinical nutrition: 4. Omega-3 fatty acids in cardiovascular care. CMAJ : Canadian Medical Association journal, 2002. 166(5):608-15.
4. Dawczynski C et al. Incorporation of n-3 PUFA and gamma-linolenic acid in blood lipids and red blood cell lipids together with their influence on disease activity in patients with chronic inflammatory arthritis--a randomized controlled human intervention trial. Lipids in health and disease, 2011. 10:130.
5. Kremer JM et al. Effects of manipulation of dietary fatty acids on clinical manifestations of rheumatoid arthritis. Lancet, 1985. 1(8422):184-7.
6. James MJ et al, Dietary n-3 fatty acids and therapy for rheumatoid arthritis. Semin Arthritis Rheum, 1997. 27(2):85-97.
7. James M et al. Fish oil and rheumatoid arthritis: past, present and future. Proc Nutr Soc, 2010. 69(3):316-23.
8. Caughey GE et al. Fish oil supplementation increases the cyclooxygenase inhibitory activity of paracetamol in rheumatoid arthritis patients. Complement Ther Med, 2010. 18(3-4):171-4.
9. Endres S et al. The effect of dietary supplementation with n-3 polyunsaturated fatty acids on the synthesis of interleukin-1 and tumor necrosis factor by mononuclear cells. N Engl J Med, 1989. 320(5):265-71.
10. Olendzki BC et al. Treatment of rheumatoid arthritis with marine and botanical oils: influence on serum lipids. Evid Based Complement Alternat Med, 2011. 2011: Article ID 827286.
11. Lerna M et al. Supplementation of diet with krill oil protects against experimental rheumatoid arthritis. BMC musculoskeletal disorders, 2010. 11:136.
12. Valensa. FlexPro MD Clinical Trial Overview and Results. (Data on File.) 2011
13. Hill WS et al. A Multicenter, Randomized, Double-Blinded, Placebo-Controlled Clinical Trial to Evaluate the Efficacy and Safety of a Krill Oil, Astaxanthin, and Oral Hyaluronic Acid Complex on Joint Health in People with Mild Osteoarthritis. Nutrients. 2023 Sep; 15(17): 3769.
14. Leventhal LJ et al. Treatment of rheumatoid arthritis with gammalinolenic acid. Ann Intern Med, 1993. 119(9):867-73.
15. Cameron M et al. Evidence of effectiveness of herbal medicinal products in the treatment of arthritis. Part 2: Rheumatoid arthritis. Phytother Res, 2009. 23(12):1647-62.
16. Leventhal LJ et al. Treatment of rheumatoid arthritis with blackcurrant seed oil. Br J Rheumatol, 1994. 33(9):847-52.
17. Macfarlane GJ et al. Evidence for the efficacy of complementary and alternative medicines in the management of rheumatoid arthritis: a systematic review. Rheumatology (Oxford), 2011. 50(9):1672-83.
18. Radovits BJ et al. Excess mortality emerges after 10 years in an inception cohort of early rheumatoid arthritis. Arthritis Care Res (Hoboken), 2010. 62(3):362-70.
19. Peters MJ et al. Does rheumatoid arthritis equal diabetes mellitus as an independent risk factor for cardiovascular disease? A prospective study. Arthritis Rheum, 2009. 61(11): 1571-9.
20. Cameron M et al. Herbal therapy for treating rheumatoid arthritis. Cochrane Database Syst Rev, 2011(2):CD002948.
21. Brzeski M et al. Evening primrose oil in patients with rheumatoid arthritis and side-effects of non-steroidal anti-inflammatory drugs. Br J Rheumatol, 1991. 30(5):370-2.
22. Talbott SM et al. The Health Professional’s Guide to Dietary Supplements. Baltimore, MD: Lippincott Williams & Wilkins; 2007. Paperback; 444 pages. ISBN-13: 978-0-7817-4672-4.
23. Rutjes AW et al. S-Adenosylmethionine for osteoarthritis of the knee or hip. Cochrane Database Syst Rev, 2009(4):CD007321.
24. Soeken KL et al. Safety and efficacy of S-adenosylmethionine (SAMe) for osteoarthritis. J Fam Pract, 2002. 51(5):425-30.
25. Nesher G et al. In vitro effects of methotrexate on polyamine levels in lymphocytes from rheumatoid arthritis patients. Clin Exp Rheumatol, 1996. 14(4):395-9.
26. Hua J et al. Evaluation of the suppressive actions of glucosamine on the interleukin-1beta-mediated activation of synoviocytes. Inflamm Res, 2007. 56(10):432-8.
27. Nakamura H et al. Effects of glucosamine administration on patients with rheumatoid arthritis. Rheumatol Int, 2007. 27(3):213-8.
28. Martinez-Calatrava MJ et al. Improvement of experimental accelerated atherosclerosis by chondroitin sulphate. Osteoarthritis Cartilage, 2010. 18 Suppl 1:S12-6.
29. Grober U et al. Vitamin K: an old vitamin in a new perspective. Dermatoendocrinol. 2014;6(1):e968490.
30. Ohsaki Y et al. Vitamin K Suppresses Lipopolysaccharide-Induced Inflammation in the Rat. Bioscience, Biotechnology, and Biochemistry. 2006;70(4):926-932.
31. Juanola-Falgarona M et al. Association between dietary phylloquinone intake and peripheral metabolic risk markers related to insulin resistance and diabetes in elderly subjects at high cardiovascular risk. Cardiovasc Diabetol. 2013;12(7).
32. Okamoto H et al. Anti-arthritis effects of vitamin K(2) (menaquinone-4)--a new potential therapeutic strategy for rheumatoid arthritis. The FEBS J. 2007;274(17):4588-94.
33. Ebina K et al. Vitamin K2 administration is associated with decreased disease activity in patients with rheumatoid arthritis. Mod Rheumatol. 2013;23(5):1001-7.
34. Rheaume-Bleue K. Choosing the Right Vitamin K2: Menaquinone-4 vs Menaquinone-7: Clinical considerations of different forms of vitamin K2. Natural Medicine Journal. 2015;7(10).
35. Gopinath K et al. Supplementation of 1,25 dihydroxy vitamin D3 in patients with treatment naive early rheumatoid arthritis: a randomised controlled trial. Int J Rheum Dis, 2011. 14(4):332-9.
36. Stoll D et al. High prevalence of hypovitaminosis D in a Swiss rheumatology outpatient population. Swiss Med Wkly. 2011 May 27;141:w13196.
37. Zwerina K et al. Vitamin D receptor regulates TNF-mediated arthritis. Ann Rheum Dis, 2011. 70(6):1122-9.
38. Cooney JK et al. Benefits of exercise in rheumatoid arthritis. J Aging Res, 2011. 2011: Article ID 681640.
39. Chiang EP et al. Abnormal vitamin B(6) status is associated with severity of symptoms in patients with rheumatoid arthritis. Am J Med, 2003. 114(4):283-7.
40. Huang SC et al. Vitamin B(6) supplementation improves pro-inflammatory responses in patients with rheumatoid arthritis. Eur J Clin Nutr, 2010. 64(9):1007-13.
41. Whittle SL et al. Folate supplementation and methotrexate treatment in rheumatoid arthritis: a review. Rheumatology (Oxford), 2004. 43(3):267-71.
42. Chiou WF et al. Mechanisms of suppression of inducible nitric oxide synthase (iNOS) expression in RAW 264.7 cells by andrographolide. Br J Pharmacol. 2000 Apr;129(8):1553-60.
43. Liu J et al. Inhibitory effects of neoandrographolide on nitric oxide and prostaglandin E2 production in LPS-stimulated murine macrophage. Mol Cell Biochem. 2007 Apr;298(1-2):49-57.
44. Liu J et al. In vivo and in vitro anti-inflammatory activities of neoandrographolide. Am J Chin Med. 2007;35(2):317-28.
45. Liu J et al. Andrograpanin, isolated from Andrographis paniculata, exhibits anti-inflammatory property in lipopolysaccharide-induced macrophage cells through down-regulating the p38 MAPKs signaling pathways. Int Immunopharmacol. 2008 Jul;8(7):951-8.
46. Bao Z et al. A novel antiinflammatory role for andrographolide in asthma via inhibition of the nuclear factor-kappaB pathway. Am J Respir Crit Care Med. 2009 Apr 15;179(8):657-65.
47. Ahn KS et al. Transcription Factor NF-{kappa}B: A sensor for smoke and stress signals. Ann N Y Acad Sci. 2005 Nov;1056:218-33.
48. Chao WW et al. Inhibitory effects of ethyl acetate extract of Andrographis paniculata on NF-{kappa}B trans-activation activity and LPS-induced acute inflammation in mice. Evid Based Complement Alternat Med. 2011:2011:254531.
49. Naik SR et al. Evaluation of immunomodulatory activity of an extract of andrographolides from Andographis paniculata. Planta Med. 2009 Jun;75(8):785-91.
50. Manganelli P et al. [Weekly low-dose methotrexate in rheumatoid arthritis. Review of the literature]. Minerva medica, 1993. 84(10):541-52.
51. Jackson JK et al. The antioxidants curcumin and quercetin inhibit inflammatory processes associated with arthritis. Inflamm Res, 2006. 55(4):168-75.
52. Henrotin Y et al. Biological actions of curcumin on articular chondrocytes. Osteoarthritis Cartilage, 2010. 18(2):141-9.
53. Buhrmann C et al. Curcumin mediated suppression of nuclear factor-kappaB promotes chondrogenic differentiation of mesenchymal stem cells in a high-density co-culture microenvironment. Arthritis Res Ther, 2010. 12(4):R127.
54. Banji D et al. Synergistic activity of curcumin with methotrexate in ameliorating Freund's Complete Adjuvant induced arthritis with reduced hepatotoxicity in experimental animals. Eur J Pharmacol, 2011. 668(1-2):293-8.
55. Deodhar SD et al. Preliminary study on antirheumatic activity of curcumin (diferuloyl methane). Indian J Med Res, 1980. 71:632-4.
56. Chandran B et al. A Randomized, Pilot Study to Assess the Efficacy and Safety of Curcumin in Patients with Active Rheumatoid Arthritis. Published online 9 MAR 2012.
57. Lee JH et al. Evaluation of antioxidant and inhibitory activities for different subclasses flavonoids on enzymes for rheumatoid arthritis. J Food Sci, 2010. 75(7):H212-7.
58. Natarajan V et al. Formulation and evaluation of quercetin polycaprolactone microspheres for the treatment of rheumatoid arthritis. J Pharm Sci, 2011. 100(1):195-205.
59. Ammon HP. Boswellic acids in chronic inflammatory diseases. Planta Med, 2006. 72(12):1100-16.
60. Banji D et al. Bioavailability, anti-inflammatory and anti-arthritic effect of Acetyl Keto Boswellic acid and its combination with methotrexate in an arthritic animal model. Journal of ethnopharmacology. Jun 28 2022;292:115200.
61. Kumar R et al. Effect of Boswellia Serrata Extract on Acute Inflammatory Parameters and Tumor Necrosis Factor-α in Complete Freund's Adjuvant-Induced Animal Model of Rheumatoid Arthritis. Int J Appl Basic Med Res. Apr-Jun 2019;9(2):100-106.
62. Sethi V et al. Potential complementary and/or synergistic effects of curcumin and boswellic acids for management of osteoarthritis. Ther Adv Musculoskelet Dis. 2022 Sep 22:14:1759720X221124545.
63. Etzel R. Special extract of BOSWELLIA serrata (H 15) in the treatment of rheumatoid arthritis. Phytomedicine. May 1996;3(1):91-4.
64. Chopra A et al. Randomized double blind trial of an ayurvedic plant derived formulation for treatment of rheumatoid arthritis. The Journal of rheumatology. Jun 2000;27(6):1365-72.
65. Shukla M et al. Consumption of hydrolyzable tannins-rich pomegranate extract suppresses inflammation and joint damage in rheumatoid arthritis. Nutrition, 2008. 24(7-8):733-43.
66. Balbir-Gurman A et al. Consumption of pomegranate decreases serum oxidative stress and reduces disease activity in patients with active rheumatoid arthritis: a pilot study. Isr Med Assoc J, 2011. 13(8):474-9.
67. Grzanna R et al. Ginger--an herbal medicinal product with broad anti-inflammatory actions. J Med Food, 2005. 8(2):125-32.
68. Nievergelt A et al. Ginger phenylpropanoids inhibit IL-1beta and prostanoid secretion and disrupt arachidonate-phospholipid remodeling by targeting phospholipases A2. J Immunol, 2011. 187(8):4140-50.
69. Funk JL et al. Comparative effects of two gingerol-containing Zingiber officinale extracts on experimental rheumatoid arthritis. J Nat Prod, 2009. 72(3):403-7.
70. Ramadan G et al. Anti-inflammatory and anti-oxidant properties of Curcuma longa (turmeric) versus Zingiber officinale (ginger) rhizomes in rat adjuvant-induced arthritis. Inflammation, 2011. 34(4):291-301.
71. Fouda AM et al. Evaluation of the effect of hydroalcoholic extract of Zingiber officinale rhizomes in rat collagen-induced arthritis. Basic Clin Pharmacol Toxicol, 2009. 104(3):262-71.
72. Tekeoglu I et al. Effects of thymoquinone (volatile oil of black cumin) on rheumatoid arthritis in rat models. Phytother Res. 2007 Sep;21(9):895-7.
73. Gheita TA et al. Effectiveness of Nigella sativa Oil in the Management of Rheumatoid Arthritis Patients: A Placebo Controlled Study. Phytother Res. 2012 Aug;26(8):1246-8.
74. Ju YH et al. beta-Sitosterol, beta-Sitosterol Glucoside, and a Mixture of beta-Sitosterol and beta-Sitosterol Glucoside Modulate the Growth of Estrogen-Responsive Breast Cancer Cells In Vitro and in Ovariectomized Athymic Mice. J Nutr. 2004 May;134(5):1145-51.
75. [Anonymous]. Monograph. Plant sterols and sterolins. Altern Med Rev. 2001 Apr;6(2):203-6.
76. Bouic P et al. The effects of B-sitosterol (BSS) and B-sitosterol glucoside (BSSG) mixture on selected immune parameters of marathon runners: inhibition of post marathon immune suppression and inflammation. Int J Sports Med. 1999 May;20(4):258-62.
77. Louw I et al. A pilot study of the clinical effects of a mixture of beta-sitosterol and beta-sitosterol glucoside in active rheumatoid arthritis (RA). Am J Clin Nutr. Feb 2002 75(2):351S-351S
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国风湿病学会
http://www.rheumatology.org
美国国立公众健康网
www.medlineplus.gov
美国关节炎基金会
http://www.arthritis.org
加拿大风湿病学协会
http://rheum.ca
加拿大关节炎病协会
http://arthritis.ca
其他参考文献:详见具体的综合干预方案
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

